В чем разница между Лекемби и Aduhelm? Простой обзор.
Последнее обновление: 19 ноября 2024 г.
Вы можете легально получить доступ к новым лекарствам, даже если они не одобрены в вашей стране.
Узнайте, какС 2021 года FDA выдало ускоренное одобрение двум новым препаратам для лечения болезни Альцгеймера. Это антиамилоидные препараты Leqembi (леканемаб) и Aduhelm (адуканумаб). Оба препарата были одобрены после почти 20 лет отсутствия серьезных прорывов в лечении болезни Альцгеймера. Благодаря этому оба препарата привлекли широкое внимание СМИ.
Однако реакция на них была неоднозначной. Мария Каррильо, главный научный сотрудник Ассоциации Альцгеймера, назвала одобрение новых препаратов "важной вехой для людей, имеющих право на это лечение" [2]. В то же время процесс их утверждения был окружен спорами, особенно в случае с Aduhelm [1, 4].
Как пациенту, вам наверняка интересно, в чем разница между Leqembi (леканемаб) и Aduhelm (адуканумаб). В этой статье мы сравним эти два препарата по принципу действия, эффективности, а также стоимости и доступности.
Лекемби против Aduhelm: Для чего они нужны?
Оба препарата предназначены для лечения ранней стадии болезни Альцгеймера. Они являются антиамилоидными препаратами и направлены на амилоидные бляшки в мозге.
Согласно инструкции по применению, Лекемби и Aduhelm предназначены для пациентов с легкими когнитивными нарушениями и подтвержденным повышенным уровнем бета-амилоида [5].
Лекемби против Aduhelm: как они работают?
Сходства
Лекемби (леканемаб) и Aduhelm (адуканумаб) - это моноклональные антитела. Они предназначены для борьбы с бета-амилоидными бляшками, которые образуются в мозге пациентов с болезнью Альцгеймера. Считается, что эти бляшки способствуют снижению когнитивных способностей и клиническому ухудшению, наблюдаемому при этом заболевании.
Оба препарата связываются с амилоидными бляшками и нейтрализуют их, чтобы замедлить прогрессирование болезни. Именно этим Лекемби и Aduhelm принципиально отличаются от предыдущих препаратов для лечения болезни Альцгеймера, таких как галантамин, ривастигмин и донепезил. Эти предыдущие препараты направлены на облегчение симптомов заболевания. Leqembi и Aduhelm направлены на изменение течения болезни, воздействуя на ее первопричину.
Различия
Leqembi и Aduhelm связываются с разными частями белка бета-амилоида. Aduhelm сильнее связывается с крупными, затвердевшими амилоидными бляшками. Leqembi, как сообщается, лучше воздействует на более мелкую, растворимую (и более токсичную) форму амилоидного белка [6].
Насколько эффективны Лекемби и Aduhelm?
Эффективность препаратов Leqembi (леканемаб) и Aduhelm(адуканумаб) была изучена в ходе клинических испытаний.
-
Результаты клинических испытаний Leqembi
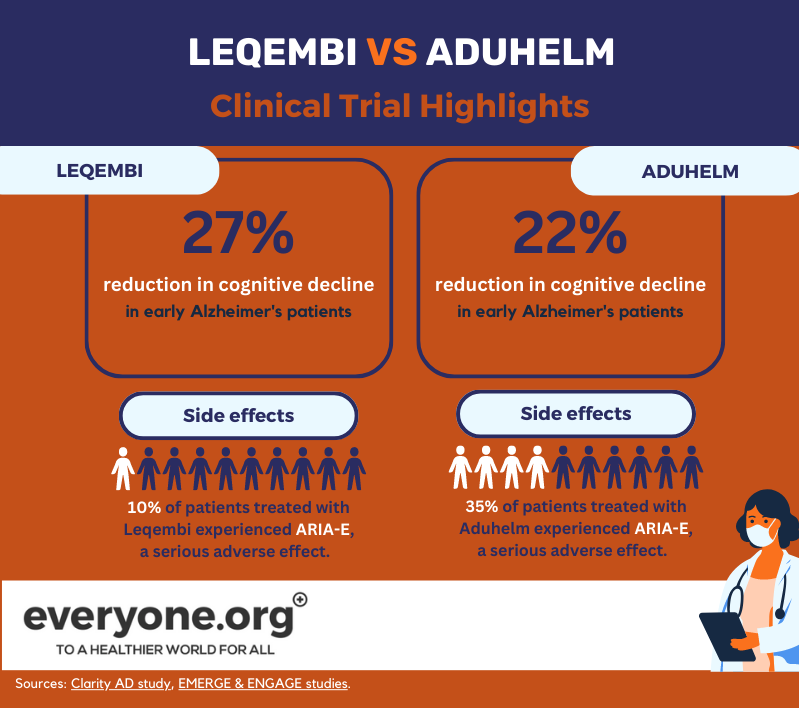
Ускоренное одобрение препарата Лекемби Управлением по контролю качества пищевых продуктов и лекарственных средств США (FDA) было основано на положительных результатах исследования 3-й фазы Clarity AD. Согласно этим результатам, леканемаб замедлил снижение когнитивных способностей на 27 % у пациентов с ранней стадией болезни Альцгеймера по сравнению с плацебо. Эти результаты были получены через 18 месяцев после начала лечения [8].
Дополнительный анализ результатов исследования был опубликован в апреле 2023 года. Он показал, что даже после того, как пациенты прекращали прием Leqembi на срок от 9 до 59 месяцев, они продолжали получать пользу от задержки снижения когнитивных способностей. В течение этого "промежуточного периода" болезнь Альцгеймера, как оказалось, прогрессировала медленнее у пациентов, принимавших Leqembi в оригинальном клиническом исследовании, по сравнению с теми, кто получал плацебо [7].
Серьезный нежелательный эффект ARIA-E возник у 10% пациентов, получавших Лекемби. У 6 % пациентов в исследовании наблюдался ARIA-H, еще один серьезный нежелательный эффект [13].
-
Результаты клинических испытаний Aduhelm
FDA выдало ускоренное одобрение Aduhelm на основании результатов двух клинических исследований 3-й фазы. Одно из них (EMERGE) показало снижение клинических показателей пациентов до 22 % [12]. В другом (ENGAGE) этого не произошло. Однако в обоих исследованиях Aduhelm продемонстрировал уменьшение количества амилоидных бляшек в мозге [9]. FDA решило, что это показание "с достаточной вероятностью приведет к клинической пользе" [10].
Подтверждающее исследование 4-й фазы (ENVISION) началось в июне 2022 года по запросу FDA. Результаты ожидаются в 2026 году [9].
Согласно информации о назначении препарата Aduhelm, 35% пациентов, принимавших препарат в клинических исследованиях, испытали ARIA-E. У 34 % пациентов, принимавших препарат в клинических исследованиях, наблюдались ARIA-H [15].
Как показывают текущие данные, основное различие между Leqembi и Aduhelm на данный момент заключается в их профиле безопасности, причем Leqembi демонстрирует более низкую частоту побочных эффектов.
В то же время, судя по текущим данным клинических испытаний, Leqembi оказывает более устойчивое воздействие на снижение когнитивных функций. Результаты текущих испытаний как Leqembi, так и Aduhelm позволят получить более четкое представление об эффективности обоих препаратов.
ПРИМЕЧАНИЕ: Представленные здесь результаты носят информационный характер и не должны служить основанием для выбора лечения. Ваш врач может определить, какое лечение лучше всего подходит именно для вашего случая.

Лекемби против Aduhelm: Безопасность и побочные эффекты
Согласно информации о назначении препарата, это наиболее распространенные побочные эффекты Leqembi (lecanemab) и Aduhelm:
Побочные эффекты Leqembi
- реакции, связанные с инфузией, включая лихорадку, гриппоподобные симптомы, тошноту, изменения частоты пульса и одышку;
- головная боль;
- Аномалии визуализации, связанные с амилоидом (ARIA) [13]. ARIA может сопровождаться временным отеком или кровоизлиянием в мозг. Симптомами ARIA являются головные боли, спутанность сознания, судороги, затрудненная ходьба и головокружение. Носители гомозиготного гена аполипопротеина Е могут быть подвержены повышенному риску развития ARIA [14].
Побочные эффекты Aduhelm
Наиболее распространенными побочными эффектами Aduhelm являются АРИЯ, головная боль и падение. Одной из побочных реакций, указанных для Aduhelm , но не для Лекемби, является гиперчувствительность. Реакции гиперчувствительности могут включать ангионевротический отек (отек глубоких слоев кожи) и крапивницу (кожная сыпь) [15].
Leqembi против Aduhelm: Сравнение цен
Если речь идет о лекарствах, которые еще не поступили в широкую продажу, любую цену следует воспринимать только как ориентировочную. Окончательная стоимость может варьироваться в зависимости от вашего местоположения, поставщиков или страхового покрытия.
Для примера, флакон Leqembi с одной дозой стоит примерно 1 043 евро. При рекомендованном приеме препарата раз в две недели годовые расходы на одного человека составят около 27 118 евро [16].
Ориентировочная цена Aduhelm за флакон с одной дозой составляет 1 335 евро. В пересчете на годовые расходы на 1 человека это составляет 34 710 евро [17].
Где утверждены Лекемби и Aduhelm ?
В настоящее время препарат Leqembi (леканемаб) одобрен только в США и Великобритании, а его одобрение EMA ожидается к концу 2024 года[3]. Лекемби также подал заявки на получение разрешения на маркетинг в Китае и Японии [18, 19, 20].
Препарат Aduhelm (адуканумаб) получил ускоренное одобрение FDA в США в июне 2021 года. Европейское агентство по лекарственным средствам (EMA) отклонило маркетинговую заявку Aduhelm в декабре 2021 года. Впоследствии заявка была отозвана компанией Biogen в апреле 2022 года [21]. Министерство здравоохранения Японии также подало негативный сигнал относительно одобрения Aduhelm в стране [22].
Leqembi или Aduhelm еще не одобрены или не доступны в вашей стране? Если вы и ваш врач считаете, что эти препараты могут принести вам пользу, свяжитесь с нашей командой экспертов по доступу к медицинским услугам. Мы предоставим вам индивидуальное ценовое предложение по поиску лекарств для вас.
Ссылки:
- Антиамилоидное моноклональное антитело леканемаб: 16 предостережений. Zenodo, 3 января 2023 года.
- Гамильтон, Джон. Управление по контролю качества пищевых продуктов и лекарственных препаратов одобрило препарат Leqembi для лечения болезни Альцгеймера в ускоренном режиме : Shots - Новости здравоохранения. NPR, 6 января 2023 года.
- Консультативный комитет FDA единогласно подтвердил клинические преимущества препарата LEQEMBI® (lecanemab-irmb) для лечения болезни Альцгеймера. Biogen | Отдел по связям с инвесторами, 9 июня 2023 г.
- Хелмор, Эдвард. FDA под огнем из-за одобрения препарата от болезни Альцгеймера Aduhelm. The Guardian, 29 декабря 2022 г.
- ОСНОВНЫЕ МОМЕНТЫ ИНФОРМАЦИИ О НАЗНАЧЕНИИ. Leqembi, Accessed 3 August 2023.
- Тейлор, Эмма. Новый препарат для лечения болезни Альцгеймера, леканемаб, попал в заголовки газет: что дальше? Alzheimer's Research UK, 13 декабря 2022 г.
- Компания Eisai: Пациенты с болезнью Альцгеймера видят преимущества Leqembi даже при прекращении приема препарата. CNBC, 6 апреля 2023 года.
- Leqembi | ALZFORUM. Alzforum, 30 мая 2023 г., Accessed 3 August 2023.
- Aduhelm | ALZFORUM. Alzforum, 6 февраля 2023, Accessed 3 August 2023.
- Каваццони, Патриция. Решение FDA одобрить новый метод лечения болезни Альцгеймера. FDA, 7 июня 2021 года.
- Компания Eisai представила полные результаты исследования III фазы Clarity AD с применением леканемаба. Alzheimer Europe, 30 ноября 2022 года.
- Основные результаты исследований EMERGE и ENGAGE: Два исследования фазы 3 по оценке адуканумаба у пациентов с ранней стадией болезни Альцгеймера. Biogen | Investor Relations, Accessed 3 August 2023.
- Идентификатор ссылки: 5105416. Accessdata.fda.gov, Accessed 3 August 2023.
- МЕДИЦИНСКОЕ РУКОВОДСТВО LEQEMBI® (leh-kem'-bee) (lecanemab-irmb) инъекция, для внутривенного применения. Leqembi, Accessed 3 August 2023.
- ОСНОВНЫЕ МОМЕНТЫ ИНФОРМАЦИИ О НАЗНАЧЕНИИ. Accessdata.fda.gov, Accessed 3 August 2023.
- Купить Leqembi (lecanemab-irmb) онлайн - цена и стоимость. Everyone.org, Accessed 3 August 2023.
- Купить Aduhelm (aducanumab-avwa) онлайн - цена и стоимость. Everyone.org, Accessed 3 August 2023.
- Компания EISAI подала заявку на получение разрешения на продажу леканемаба в качестве средства лечения ранней стадии болезни Альцгеймера в Европе | Biogen. Biogen | Отношения с инвесторами, 10 января 2023 г.
- Eisai начинает подачу данных по леканемабу в Китай | Biogen. Biogen | Investor Relations, 22 декабря 2022 г.
- Карвальо, Тереза и Рэй Буроу. Леканемаб для лечения ранней стадии болезни Альцгеймера будет представлен на рассмотрение в Японии. Alzheimer's News Today, 14 марта 2022 года.
- Обновленная информация о подаче регуляторной заявки на адуканумаб в Европейском Союзе | Biogen. Biogen | Investor Relations, 22 апреля 2022 г.
- Свифт, Роки, и др. Препарат Eisai-Biogen от болезни Альцгеймера трудно оценить - Министерство Японии. Reuters, 22 декабря 2021 г.